LCR
- 1. LCR1
- 2. Índice LCR2 Sistema nervioso Líquido Cefalorraquídeo Interés clínico LCR Toma de muestras Análisis de LCR.
- 3. LCR3 El encéfalo comprende: El cerebro que representa el 80% de la masa cerebral, El tallo cerebral. El cerebelo. La médula espinal se extiende desde el encéfalo hasta la primera vértebra lumbar por el interior del conducto de la columna vertebral. Sistema nervioso: Central: encéfalo y médula espinal. Periférico: nervios craneales y espinales.
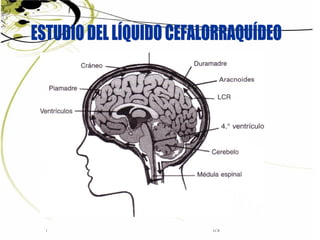
- 5. LCR5 Paquimeninge o Duramadre: es la capa más externa y resistente. Rodea a todo el SNC. Está separada de las paredes del conducto raquídeo por el espacio extradural o epidural, no existiendo ese espacio en el cráneo. Leptomeninges: aracnoides y piamadre. Están unidas por trabéculas conjuntivas y el espacio que queda entre ellas es el espacio leptomeníngeo o subaracnoideo que está lleno de LCR.
- 6. LCR6 Está constituido por los nervios. Estos pueden ser de dos tipos: craneales y raquídeos Las fibras nerviosas pueden ser aferentes o eferentes. Las fibras eferentes pueden ser: -Estriomotoras -Lisomotoras -Secretoras
- 7. LCR7 Fluido acuoso y transparente que se encuentra en el espacio subaracnoideo, entorno al encéfalo y médula espinal, y dentro de las cavidades del cerebro (ventrículos) y de la médula espinal (conducto ependimario). Toma de Muestras 7 En el adulto se produce 500 mL/ día, lo que supone unos 20 mL/h. Las células del epéndimo son células epiteliales que recubren el canal del epéndimo, incluyendo los ventrículos cerebrales y el canal neural de la médula espinal. Las células coroideas son células epiteliales que recubren el plexo coroideo. Las células coroideas junto al epitelio de los capilares forman la barrera hematoencefálica. Las células mesoteliales de la aracnoides y la piamadre son células epiteliales que las recubren.
- 8. LCR8 En el interior de la masa del encéfalo se encuentran los ventrículos. Anatómicamente son cuatro cavidades comunicadas que contienen un plexo coroideo constituido por haces de material membranoso, muy contorneado y vascularizado que produce el líquido cefalorraquídeo. Existen 2 ventrículos laterales, un tercer ventrículo y un cuarto ventrículo, comunicado este último con el espacio subaracnoideo, y que se continúa por abajo con el espacio central de la médula espinal
- 9. LCR9 El LCR se forma por filtración de sangre a través de los capilares coroideos, seguido del transporte activo de sustancias a través del epitelio coroideo hacia el ventrículo. A continuación, se registra un flujo pasivo de agua para mantener el equilibrio osmótico Durante su recorrido, la mayor parte de este líquido es reabsorbido por la sangre a través de las vellosidades aracnoideas y a través de las paredes de los capilares del S.N.C. y la piamadre. El LCR formado rellena los ventrículos, sale por las aberturas del cuarto ventrículo y se dirige hacia los hemisferios cerebrales desplazándose lentamente sobre ellos. Además, parte del LCR se desplaza, hacia el espacio subaracnoideo que rodea la médula espinal.
- 10. LCR10
- 11. LCR11
- 12. LCR12
- 13. LCR13 Actuar como fluido protector para evitar posibles lesiones del encéfalo y la médula espinal. Servir de medio de transferencia de sustancias entre la sangre y los tejidos nerviosos, es decir, actuar como regulador del medio extracelular de las neuronas. El volumen del LCR en los adultos es de aprox 90 a 150 ml de los cuales: 20 ml se encuentran en los ventrículos. 60 ml en los espacios subaracnoideos 70 ml en el canal raquídeo. • La velocidad de formación en los adultos es de unos 500 ml/día o 20 ml/hora
- 14. LCR14 • La mayor parte de los componentes del LCR existe en la misma o en menor concentración que en el plasma sanguíneo, pero hay que tener en cuenta que el líquido cefalorraquídeo no es un ultrafiltrado del plasma. • Existe por tanto, un transporte activo entre la sangre, líquido cefalorraquídeo y cerebro, en ambas direcciones, lo que da lugar a que existan concentraciones diferentes de sustancias en cada lugar. • Sin embargo, ciertas enfermedades pueden hacer que algunos elementos que normalmente no atraviesan la barrera hematoencefálica, penetren en el LCR, de ahí la necesidad de su estudio para el diagnóstico de estas enfermedades. ndicee
- 15. LCR15 El LCR se obtiene habitualmente por punción lumbar a nivel del cuarto espacio lumbar, introduciendo la aguja en el espacio subaracnoideo Antes de la extracción de cualquier cantidad de líquido, debe medirse la presión, permitiendo que el LCR llene un manómetro graduado estéril. La presión inicial normal varía entre 90 y 180 mm de agua, del LCR, determinada con el paciente en decúbito lateral. (no debe haber una caída importante de la presión porque sugiere una herniación cerebelosa o una compresión de la médula raquídea por encima del lugar de la extracción
- 16. Toma de muestras LCR16 • Las indicaciones para una punción lumbar son las siguientes: El diagnóstico de la meningitis (bacteriana, fúngica, micobacteriana y amébica), El diagnóstico de hemorragia (subaracnoidea, intracerebral e infarto cerebral), El diagnóstico de enfermedades neurológicas, tales cómo: esclerosis múltiple, enfermedades desmielinizantes y el síndrome de Guillain-Barré, El diagnóstico y evaluación de una sospecha de malignidad, tal como leucemia, linfoma y carcinoma metastásico La introducción de fármacos, medios de contraste radiográficos y anestésicos.
- 17. Toma de muestras LCR17 • Valorar ventajas frente a riesgos. • Los riesgos posibles son: Cefalea Herniación amigdalar, en caso de presión intracraneal elevada. Paresias- parálisis incompletas- en paciente con tumor de médula ósea. Meningitis en pacientes con sepsis. Muerte por asfixia en niños, por obstrucción Se realizará preferentemente por la mañana, en ayunas. Las razones son: Por la mañana en el laboratorio existe más personal, y personal más entrenado para este tipo de determinaciones. Los niveles de la glucosa en el LCR pueden evaluarse mejor por comparación con la glucosa sanguínea en ayunas.
- 18. Toma de muestras LCR18 Por lo general, se depositan 3 muestras en tubos estériles etiquetados secuencialmente como: nº 1 (estudios químicos e inmunológicos (es conveniente que contenga FNa para minimizar la posible glucólisis). nº 2 (examen microbiológico). Mantener a 37 ºC nº 3 (recuento celular y recuento diferencial (debe contener 1 gota de heparina para evitar que se formen agregados). Índice
- 20. Examen físico. Aspecto LCR20 Normal: como agua de roca. Se considera anormal cuando aparece turbio, empañado, opalescente o sanguinolento La turbidez se clasifica en una escala de 0 a 4 cruces que comprende desde la ausencia de turbidez (valor 0), hasta la imposibilidad de distinguir letras a través del tubo (valor 4+). 0= líquido transparente 1+= ligeramente turbio, "ahumado" o "empañado" 2+= turbidez claramente presente, aunque puede leerse fácilmente una hoja de periódico a través del tubo. 3+= la letra no puede leerse fácilmente a través del tubo. 4+= la letra impresa no puede percibirse a través del tubo.
- 21. Examen físico. Aspecto LCR21 La turbidez puede ser debida a: Leucocitos: se requiere un mínimo de 200 células/microlitro para provocar una ligera turbidez. Eritrocitos: por lo menos se requieren 400células/microlitro para provocar una ligera turbidez. Microorganismos: bacterias, hongos, amebas. Color. Normal: Incoloro. Alteraciones: –Una coloración rojiza indica presencia de hematíes, que deberemos diferenciar si son debidos a una hemorragia patológica o si se trata de una hemorragia traumática por la propia punción. –Un color rosa pálido o amarillo pálido del sobrenadante tras la centrifugación (líquido xantocrómico) sugiere que hay pigmentos debidos a la degradación de la hemoglobina como oxihemoglobina, metahemoglobina, bilirrubina.
- 22. Examen físico. Aspecto LCR22 En los tubos que figuran en A- líquido cefalorraquídeo de color normal. En los tubos que figuran en B- LCR hemorrágico. En los tubos D- hemorragia debida a punción, vemos que se aclara paulatinamente. En tubos C. Xantocromía.
- 23. Examen físico LCR23 Análisis de LCR.
- 24. Examen citológico LCR24 • Muestra: de 2-4 mL. • Antes de pasar 1 h desde la extracción. • No centrifugar ni diluir, pero homogeneizar. • Se realiza en todas las muestras. Células del LCR. Escasas y son: Leucocitos mononucleares- linfocitos y monocitos. Células plasmáticas. Células malignas. Células gliales. Células ependimarias. Células del plexo coroideo.
- 27. Técnica de recuento manual LCR27 • Preparar la muestra: Homogeneizar la muestra. Si la muestra es clara no diluir. Si la muestra es turbia, diluir en líquido de Türk: • Ácido acético glacial... ...................... 3 ml • Violeta de genciana al 1% ................ 1 ml • H20 destilada c.s.p....... ..................... 100 mL. Llenar la cámara de recuento. Verificar que la muestra está correctamente distribuida con objetivo 10X
- 28. Técnica de recuento manual LCR28 Cámara de Neubauer Los leucocitos se cuentan en los 4 cuadros grandes de las esquinas de 1 mm2. En el caso de que existan leucocitos sobre las líneas de demarcación del cuadrado únicamente se cuentan los de 2 de las 4 líneas (por ejemplo, superior y derecha). Cámara de Fuchs-Rosenthal con un retículo de mayor superficie (16 mm2) y el doble de altura (0,2 mm) lo que favorece el recuento de un mayor número de células.
- 29. Recuento diferencial LCR29 Cuando el recuento celular es superior a 30 leucocitos/ L, debe hacerse un recuento diferencialμ de células. Consiste en indicar el porcentaje de células mononucleares y polimorfonucleares presentes en la muestra estudiada así como otras células que pueden presentarse. La diferenciación puede hacerse: Por observación en fresco con contraste de fases. Por observación microscópica de un frotis teñido, en cuyo caso puede identificarse cualquier célula presente.
- 30. Recuento diferencial LCR30 • Pasos a seguir: Si se precisa, concentrar la muestra. Por centrifugación suave de la muestra durante 3000 rpm durante 5 minutos y posterior tinción. Mediante el empleo de membranas de filtración Millipore o similares. Con citocentrífuga. Es un método directo de extensión que utiliza la fuerza centrífuga. Se obtienen extensiones uniformes de las células sobre los portaobjetos. Tinción. Pueden emplearse diferentes tinciones: simples, May Grumwald-Giemsa, Wright, Samson, etc. Observación microscópica con objetivo de inmersión. Contar 100 células e indicar el porcentaje de poli y monomorfonucleares.
- 31. Recuento de hematíes LCR31 Sólo se realiza cuando sea necesario hacer una corrección de los leucocitos o proteínas, debido a que tanto unos como otros se han introducido de forma artificial a causa de una punción traumática. Se dice que aproximadamente para sangre periférica normal se descuenta 1-2 leucocitos por cada 1000 hematíes/µl que contemos y vamos a descontar 1 mg / dl de proteínas por cada 1200 hematíes/µl, también suponiendo que el hematocrito y el nivel sérico de proteínas es normal.
- 32. Resultados patológicos de la citología LCR32 RECUENTO TOTAL Patologías asociadas Pleocitosis moderada 10-30 células/mm3 Meningitis tuberculosa Encefalitis Tumores del SNC Pleocitosis acentuada 100-10.000 células/mm3 Meningitis purulentas Pleocitosis extrema hasta 50.000 células/mm3 Roturas de abscesos cerebrales
- 33. Resultados patológicos de la citología LCR33 RECUENTO DIFERENCIAL Patologías asociadas Predominio de neutrófilos Meningitis purulenta Predominio de linfocitos Meningitis tuberculosa y bacteriana tratada Meningitis víricas y sifilítica Meningitis micóticas Síndrome de Guillain Barré (polirradiculoneuritis Presencia de eosinófilos Meningitis de origen parasitario Presencia de células plasmáticas con linfocitos Procesos inflamatorios crónicos Esclerosis múltiple Presencia de histiocitos malignos con linfocitos Tumores cerebrales Presencia de macrófagos Infartos craneales Sustancias extrañas en LCR Análisis de LCR.
- 34. Examen bioquímico LCR34 • Se necesitan entre 0,5-1 mL. • Comprende el estudio de los metabolitos presentes en el LCR. • Las pruebas más importantes son: • La glucorraquia (concentración de glucosa en LCR). • Proteinorraquia, incluyendo el valor de la cantidad de albúmina. • Otras pruebas: • Ácido láctico • Enzimas: • LDH • CK • ADA • AST
- 35. Examen bioquimico LCR35 • Las proteínas del LCR tienen dos orígenes: • difusión desde la sangre. • Síntesis en el interior del SNC. • Como el LCR normal es principalmente un ultrafiltrado plasmático contiene muy pocas proteínas, siendo la relación albúmina/globulinas superior a la del plasma, ya que la albúmina por su menor tamaño atraviesa libremente la barrera sangre-LCR. • Las proteínas que se encuentran en el LCR son prealbúmina, albúmina, 2-macroglobulina, fibrinógeno,α transferrina, ceruloplasmina e inmunoglobulinas. • Las cifras normales de proteínas totales en una muestra obtenida por punción lumbar oscilan entre 0,15 y 0,45 g/L o 15-45 mg/dL.
- 36. Examen bioquímico. Proteinorraquia LCR36 Proteinorraquia Patologías Causas AUMENTO Siempre que hay sangre y pus Hemoglobina Proteínas plasmáticas Proteínas celulares Exudado por meninges inflamadas AUMENTO LIGERO' Inflamación de tejidos cerebrales Esclerosis múltiple Encefalitis, polineuritis Meningitis tuberculosa y luética Alteraciones vasculares Procesos tumorales Exudación por la inflamación Aumento del contenido celular Obstrucción de la circulación AUMENTO IMPORTANTE Bloqueo del canal espinal Meningitis infecciosas Abscesos cerebrales Síndrome de Guillain-Barré Bloqueo del canal espinal Meningitis infecciosas Abscesos cerebrales Síndrome de Guillain-Barré
- 37. Patrón electroforético de proteínas de LCR. LCR37
- 39. Examen bioquímico. Proteinorraquia LCR39 Figura 1. Bandas oligoclonales en la esclerosis múltiple. A: suero del paciente, B: líquido cefalorraquídeo del paciente. C: control con una gammapatía monoclonal. El líquido cefalorraquídeo del paciente contiene dos bandas distintas que no aparecen en el suero. Se observa una banda prominente de prealbúmina. La banda de transferrina, representa la transferrina desializada, también llamada proteína tau y β2-transferrina, es de mayor densidad y migra hacia la región gamma, hecho característico del líquido cefalorraquídeo. La pequeña cantidad de transferrina dializada apenas se observa en este gel de agarosa.
- 41. Examen bioquímico- Glucosa LCR41 La concentración de glucosa en LCR de adultos es aproximadamente la mitad de los niveles sanguíneos (50-80 mg/dl) y sigue los cambios de la glucemia por lo que debe obtenerse una muestra de glucosa sanguínea antes de la punción lumbar para hacer la comparación. La concentración de glucosa en el LCR puede determinarse con cualquiera de los métodos de determinación de glucosa, siendo los más adecuados los métodos enzimáticos de glucosaoxidasa/peroxidasa o de la hexoquinasa/glucosa-ó-fosfato-deshidrogenasa.
- 42. Variaciones en la glucorraquia LCR42 Glucorraquia Patologías DISMINUIDA Meningitis purulentas Meningitis tuberculosa Carcinomas meníngeos Hipoglucemia NORMAL Infeciones virales Meningitis no infecciosa AUMENTADA Diabetes mellitus
- 43. Examen bioquímico- Ácido láctico LCR43 • La concentración del ácido láctico del LCR es en gran medida independiente de los niveles sanguíneos. • La fuente principal de ácido láctico del LCR es el metabolismo anaerobio del SNC. • Valores aumentados en: • Meningitis bacterianas. • Infarto cerebral. • Tumores del SC • Cualquier situación que provoque hipoxia en el tejido del SNC.
- 44. Examen bioquímico- Enzimas LCR44 La LDH (lactato deshidrogenasa) tiene tres orígenes: difusión desde la sangre difusión desde el SNC y las células del LCR (leucocitos, gérmenes, células tumorales). Debido a esto, la determinación de esta enzima se ha utilizado para el diagnóstico diferencial de la meningitis bacteriana y vírica aunque también aumenta en otras patologías como hemorragias subaracnoideas, leucemias, linfomas o carcinomas metastásicos del SNC.
- 45. Examen bioquímico- Enzimas LCR45 • La actividad de la CK (creatínkinasa) aumenta en múltiples trastornos del SNC por lo que se considera indicativa de enfermedad neurológica pero inespecífica. Cuando se encuentra por encima de 4U/L indica lesión cerebral isquémica. • La determinación de la enzima ADA (adenosindesaminasa) es de gran utilidad en el diagnóstico de la meningitis tuberculosa ya que los valores superiores a 9 U/L son muy específicos de esta enfermedad. • La AST (aspartato aminotransferasa) aumenta en meningitis, hemorragias y tumores. Análisis de LCR.
- 46. EXAMEN BACTERIOLÓGICO Y SEROLÓGICO LCR46 Se necesita una cantidad mayor de 2 mL. Se realizan tinciones rápidas: `Gram tinta china para bácilos ácido alcohol resistentes
- 47. EXAMEN BACTERIOLÓGICO Y SEROLÓGICO LCR47 También se hacen pruebas de aglutinación en látex para el diagnóstico de la presencia de bacterias habituales. Cultivo: bacterias (anaeróbico, aeróbico), virus, micobacterias, hongos Reacción en cadena de la polimersa (PCR): algunos organismos virales (virus del herpes simple), tuberculosis VDRL: neurosífilis
- 48. Parámetros de análisis del LCR en diversas patologías LCR48 Meningitis: Meningitis bacteriana aguda: Elevado número de neutrófilos. Elevado número de linfocitos. Elevación de las fracciones 3 y 4 de la LDH. Elevación del lactato. Encefalitis viral La amplificación por PCR de los ácidos nucleicos virales se ha convertido en el procedimiento diagnóstico de elección para muchos tipos de encefalitis viral. La PCR es hoy día la prueba diagnóstica principal para las infecciones del sistema nervioso central producidas por citomegalovirus, virus Epstein- Barr, virus varicela zoster y enterovirus.
- 49. Parámetros de análisis del LCR en diversas patologías LCR49 Esclerosis múltiple En la mayoría de los pacientes con esclerosis múltiple se observa un índice IgG / albúmina mayor de 0,27, un índice IgG mayor de 0,7 y una tasa de síntesis de IgG mayor de 8. Para el diagnóstico de esclerosis múltiple se hace un estudio de bandas oligoclonales por electroforesis. Para descartar la posibilidad de que el paciente tenga una gammapatía monoclonal que aparecería en el líquido cefalorraquídeo, debe realizarse paralelamente un proteinograma en suero. En el 75 al 90 % de los pacientes se identifican dos o más bandas oligloconales.
- 50. Parámetros de análisis del LCR en diversas patologías LCR50 Enfermedad de Creutzfeldt-Jacob En el diagnóstico de la demencia, el uso de la evaluación de la proteína 14-3-3 en el líquido cefalorraquídeo se ha considerado útil para confirmar o rechazar el diagnóstico de enfermedad de Creutzfeldt-Jacob. Concentraciones elevadas de esta proteína neuronal se ha encontrado que correlacionan razonablemente bien con el desarrollo de la enfermedad de Creutzfeldt-Jacob. Sin embargo, elevaciones de la proteína 14-3-3 en líquido cefalorraquídeo también están presentes en casos de infarto y encefalitis y ocasionalmente en pacientes con enfermedad de Alzheimer, demencia fronto-temporal, enfermedad de Lewy y meningitis carcinomatosa, de tal forma que la interpretación debe hacerse con cautela.
- 51. Parámetros de análisis del LCR en diversas patologías LCR51 Hemorragia subaracnoidea Diferenciar con punción traumática, por color y aclaramiento de los tubos, centrifugación y la presencia o ausencia de xantocromía. Aparte de lo ya indicado, se ha demostrado que la cuantificación espectrométrica de productos de la degradación de la hemoglobina es una herramienta útil para el diagnóstico diferencial. Algunos estudios sugieren que la determinación del dímero-D sería importante en el diagnóstico diferencial de la punción lumbar traumática (negativo) y de la hemorragia subaracnoidea (positivo) y posiblemente de otras hemorragias intracraneales.
- 52. Parámetros de análisis del LCR en diversas patologías LCR52 Encefalopatía hepática En el sistema nervioso central una gran proporción del amonio es secuestrado por el -cetoglutarato paraα formar glutamina. El intervalo de referencia de glutamina en líquido cefalorraquídeo es de 0,3 a 1,4 mmol/L, concentraciones superiores a 2,45 mmol/L casi siempre se asocian con síntomas de encefalopatía metabólica. El coma hepático puede verse con concentraciones entre 1,75 y 6,65 mmol//L.
- 53. LCR LCR53
Editor's Notes
- Se atribuye su descubrimiento a Cotugno en 1784. Arranz, 249. Los ventrículos cerebrales son: Ventrículos laterales: situados en cada hemisferio cerebral. Son los que más producen LCR. Tercer ventrículo: debajo y detrás del ventrículo lateral. Cuarto ventrículo: en donde el cerebelo se adosa a la cara posterior del tronco encefálico. Thibodeau, 377. La mayor parte de los 150 cc, 100, se encuentra en el espacio subaracnoideo. Algunos autores dicen que el ritmo de la reabsorción es de 6 a 7 veces cada 24 horas; otros dicen que la renovación total ocurre solo al cabo de dos semanas. Arranz, 249. En niños, el volumen es de 10-60 ml. Paraninfo, 296.
- Thibodeau, 380.
- Variaciones del CO2 desencadenan respuestas homeostáticas en los centros de control respiratorio del encéfalo que ayudan a regular el contenido total de CO2 y pH del cuerpo. Thibodeau 377 y Tortora 455.