SINDROME WISKOTT-ALDRICH
- 1. CASO CLÍNICO - SÍNDROME DE WISKOTT-ALDRICH Andrea Carrascal Herazo Medicina V 2014
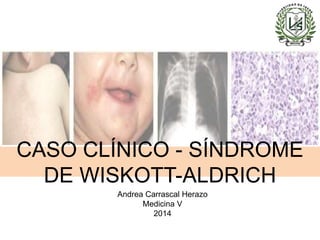
- 2. SÍNDROME DE WISKOTT-ALDRICH Inmunodeficiencia primaria ligada al cromosoma X Microtrombocitopenia congénita Ezcema Infecciones recurrentes
- 3. SÍNDROME DE WISKOTT-ALDRICH 1 a 10 en un millón de recién nacidos vivos y la expectativa de vida es de 15 años Gen WASP Síndrome de Wiskott-Aldrich Células hematopoyéticas
- 4. CASO CLÍNICO Padres aparentemente sanos y tío materno finado a los tres meses de edad por sepsis de foco pulmonar. Hijo de primera gestación- No tuvo control prenatal Parto vaginal en unidad hospitalaria a las 27 semanas de gestación Tuvo un peso de 1,400 gr- Hospitalizado a los dos meses de vida
- 5. CASO CLÍNICO • El paciente egresó pesando 2,200 gr. • Se contraindicó la aplicación de todo tipo de inmunizaciones.
- 6. CASO CLÍNICO En 8 ocasiones fue tratado con inmunoglobulina intravenosa y factor de transferencia Hospitalizado en 54 ocasiones A los tres años también padeció dermatitis atópica
- 7. CASO CLÍNICO Fue referido a un hospital de tercer nivel, en el que fue hospitalizado para que recibiera un trasplante de médula ósea. · Edad aparentemente menor a la cronológica · Peso y talla por debajo del percentil 5 · Dolicocéfalo · Cabello bien implantado · Lesiones dérmicas caracterizadas por pápula eritematosas · Múltiples caries y abundante placa dentobacteriana en l cavidad oral · Cuello cilíndrico con ganglios palpables de 0.5 cm en l región cervical · Tórax normolíneo con adecuada entrada y salida de aire · Ruidos cardiacos rítmicos de adecuada intensidad y si agregados.
- 8. CASO CLÍNICO · Abdomen blando, depresible y no doloroso a la palpació · Sin hepatomegalia ni esplenomegalia · Perístalsis normal · Extremidades con hipotrofia muscular · Llenado capilar y pulsos normales · Genitales normales para la edad · Piel con dermatosis diseminada en la cabeza, tronco y extremidades · Piel sin dermatosis en las palmas y las plantas · Espalda con petequias · Extremidades con estigmas de rascado, costras hemáticas, equimosis. · Zonas de dermatitis perianal · Psicomotricidad con retraso para su edad.
- 9. CASO CLÍNICO · Hemoglobina de 8.1 g/dL · Trombocitopenia de 31,000/uL y volumen plaquetario de 5.6 fL · Grupo sanguíneo A y factor RH+ · IgM 39.3 mg/dL (47-200 mg/dL), IgA 67 mg/dl (22-159 mg/ dL), IgG 1,380 mg/dl (441-1,135 mg/dl). · Gastroenteritis infecciosa y otitis crónica ceftriaxona y clindamicina intravenosa. · Cada 21 días le aplicaron gammaglobulina intravenosa a 400mg/kg.
- 10. CASO CLÍNICO El trasplante de médula ósea se postergó por complicaciones, que ameritaron 13 hospitalizaciones Plaquetopenia severa Múltiples infecciones Sangrado de tubo digestivo bajo Artritis séptica Gastroenteritis infecciosa Otitis media supurada crónica Foliculitis severa
- 11. CASO CLÍNICO A la edad de 4 años 7 meses el paciente recibió –trece meses después de su ingreso– el trasplante de médula ósea, para lo cual fue preparado con busulfán y ciclosfosfamida. El cordón fue compatible con el paciente en 5/6 antígenos, la transfusión ocurrió sin incidentes y la nutrición se inició en forma parenteral. Hubo respuesta inflamatoria sistémica a los cuatro días del trasplante y se realizó en el catéter central un cultivo, el cual fue positivo para bacterias grampositivas, por lo que el paciente fue tratado con clindamicina, meropenem y vancomicina. Posteriormente, el paciente tuvo dificultad respiratoria secundaria a neumonía nosocomial por Staphylococcus aureus, por lo que ameritó intubación endotraqueal. 26 días después del trasplante falleció por choque séptico.
- 12. Regulado r Membrana plasmática Migración celular Movilización celular Actina Miosina Polimeriz ación SINDROME DE WISKOTT-ALDRICH Gen WASP Síndrom e de Wiskott- Aldrich Células hematopoy éticas
- 13. SINDROME DE WISKOTT-ALDRICH • Estudiaron la respuesta inmunitaria de pacientes con síndrome de wiskott-Aldrich. Cuando inmunizaron a estos pacientes con un bacteriófago, éstos no produjeron anticuerpos en forma normal; específicamente, tuvieron un defecto en el cambio de isotipo e incapacidad para desarrollar memoria inmunológica • Las concentraciones de inmunoglobulinas son normales en pacientes con este síndrome. Justifica la administración de inmunogammaglobulina G intravenosa. • Las diferentes mutaciones en el gen WASP producen espectros clínicos diferentes. Se han descrito el síndrome de wiskott-Aldrich clásico (susceptibilidad a infecciones, trombocitopenia y eccema), la trombocitopenia intermitente o ligada al cromosoma X y la
- 14. DIAGNÓSTICO · El síndrome de wiskott-Aldrich debe sospecharse en varones con sangrado asociado con eccema severo o moderado. · El diagnóstico se corrobora con exámenes de laboratorio. · Por citometría de flujo el número de linfocitos circulantes puede ser normal, estar discreta o moderadamente disminuido. · Las concentraciones de IgG se encuentran frecuentemente en rango normal; la IgM está disminuida y las inmunoglobulinas IgA e IgE se encuentran elevadas. · El diagnóstico definitivo es detectar la mutación en el gen WASP.
- 15. TRATAMIENTO Los tratamientos iniciales que mejoran el pronóstico de los pacientes con síndrome de wiskott-Aldrich · Transfusión de plaquetas · Administración de inmunogammaglobulina G intravenosa · Esplenectomía · Profilaxis con antibióticos y antivirales El tratamiento contra el eccema requiere esteroides El trasplante de médula ósea es el único tratamiento curativo. La esplenectomía está indicada para disminuir la plaquetopenia severa y para casos en los que no pueda realizarse el trasplante de médula ósea.
- 16. CONCLUSIÓN • El síndrome de wiskott-Aldrich es una inmunodeficiencia primaria severa con un fenotipo clínico variable. • Se ha reportado que los defectos celulares ocasionados por la mutación en el gen WASP son la causa del fenotipo inmunológico. • Los pacientes con síndrome de wiskott-Aldrich pueden vivir hasta la edad adulta; sin embargo, una proporción significativa fallece por hemorragia, infección, enfermedad maligna o complicaciones posteriores al trasplante de médula ósea. • En síndrome de wiskott-Aldrich y en otras inmunodeficiencias primarias el pronóstico del trasplante de médula ósea depende de que éste se realice en etapas tempranas de la vida. • Es importante comunicar a los médicos de primer contacto los signos y síntomas iniciales de las inmunodeficiencias primarias, como lo son las infecciones recurrentes y severas, para que sean diagnosticadas y tratadas oportunamente.
Editor's Notes
- Las manifestaciones clínicas generalmente ocurren al nacimiento y consisten en petequias, equimosis, sangrado del tubo digestivo bajo, epistaxis y hemorragia intracraneal. La existencia de infecciones severas desde el nacimiento es un dato importante para establecer dichos diagnósticos. 6. • El eccema, una manifestación característica durante la lactancia y la infancia, persiste hasta la edad adulta; en la mayoría de los casos se manifiesta en forma grave y resiste al tto Los pacientes afectados padecen una combinación deinmunodeficiencia humoral y celular, que se manifiesta por susceptibilidad a infecciones recurrentes
- Se estima que su incidencia en el mundo es de 1 a 10 en un millón de recién nacidos vivos y la expectativa de vida es de 15 años sin trasplante de médula ósea.1,2 Es causado por una mutación en el gen WASP, que codifica para la proteína del síndrome de Wiskott-Aldrich, presente sólo en las células hematopoyéticas.
- Hospitalizado en 54 ocasiones por sangrado del tubo digestivo bajo y epistaxis asociada con choque hemorrágico, gingivorragia, infecciones dentales e infecciones respiratorias, como otitis media crónica, sinusitis y neumonía; en ocho ocasiones fue tratado con inmunoglobulina intravenosa y factor de transferencia. A los tres años también padeció dermatitis atópica Fueron descubiertos por el Dr. H. Sherwood Lawrence mientras investigaba la tuberculosis. Descubrió que podía transferirse una respuesta inmune de un donante a un receptor inyectando un extracto de leucocitos. El Dr. Lawrence bautizó a esta sustancia Factor de Transferencia en inglés "Transfer Factor" que es el término empleado universalmente por los científicos. Se ha determinado que el Transfer Factor aislado es un pequeño péptido que actualmente ya se ha descubierto que cuenta con más de 18 residuos de aminoácidos que combinados pueden crear millones de distintos Factores de Transferencia. Estas microscopicas moléculas de Factor de Transferencia contienen únicamente la "Esencia del Mensaje Inmunológico." Este mensaje es transferido de la madre al hijo a través del Calostro, primera leche que segregan todos los mamíferos, incluidos los humanos, durante tres días después de dar a luz. Podriamos definir metafóricamente a los Factores de transferencia como Micro-chips del sistema Inmune porque transfieren INFORMACIÓN GENÉTICA de cómo la madre y generaciones anteriores se han defendido de virus, bacterias , hongos , parásitos y células anómalas. El Factor de Transferencia contenido en el calostro tiene tres funciones y habilidades específicas: 1.RECONOCER: TRANSFIERE INFORMACIÓN AL SISTEMA INMUNE DEL BEBÉ PARA EDUCAR SU SISTEMA INMUNE Y QUE SEPA RECONOCER A LOS AGENTES PATÓGENOS. 2.RESPONDER: LE TRANSFIERE LA CAPACIDAD DE RESPUESTA ADECUADA A CADA PATÓGENO INCLUYE LA CAPACIDAD DE MODULAR LA RESPUESTA CUANDO EL SISTEMA INMUNE SOBREREACCIONA DEFENDIÉNDOSE DE AGENTES NO PATÓGENOS= ALERGIAS. O CUANDO EL SISTEMA INMUNE SE AGREDE A SI MISMO=RESPUESTA AUTOINMUNE. 3.RECORDAR: CAPACIDAD DE RECORDAR QUÉ AGENTES DEBE ATACAR, CÓMO Y DE QUÉ MANERA. El calostro es un líquido secretado por las glándulas mamarias durante el embarazo y los primeros días después del parto, compuesto por inmunoglobulinas, agua, proteínas, grasas y carbohidratos en un líquido seroso y amarillo. "Para el nacimiento del bebé se preparara uno de los alimentos más importantes de su vida, el calostro. Este alimento es la primera leche que se produce y su duración está entre los 2 y 5 días, antes de que se empiece a producir la leche definitiva. El calostro es un alimento ideal y primordial, ya que en él está la primera inmunización del bebé y resuelve además las necesidades alimentarias de sus pequeños órganos, aún no maduros.
- Lesiones dérmicas caracterizadas por pápulas eritematosas, que confluían y formaban en los pabellones auriculares placas excoriadas con liquenificación y edema
- Los resultados de laboratorio fueron: hemoglobina de 8.1 g/dL, trombocitopenia de 31,000/uL y volumen plaquetario de 5.6 fL (en varias ocasiones le transfundieron paquetes globulares y concentrados plaquetarios). Grupo sanguíneo A y factor RH+, aglutinina anti-A negativa, aglutinina anti-B 1: 4, Coombs directo negativo, IgM 39.3 mg/dL (47-200 mg/dL), IgA 67 mg/dl (22-159 mg/ dL), IgG 1,380 mg/dl (441-1,135 mg/dl). Durante 16 días de hospitalización el paciente tuvo gastroenteritis infecciosa y otitis crónica, porlo que recibió tratamiento con ceftriaxona y clindamicina intravenosa. Luego, cada 21 días le aplicaron gammaglobulina intravenosa a 400 mg/kg/dosis e inmunizaciones (neumococo heptavalente y vacuna DPT acelular
- El trasplante de médula ósea se postergó por complicaciones, que ameritaron 13 hospitalizaciones por plaquetopenia severa asociada con sangrado de tubo digestivo bajo y múltiples infecciones (artritis séptica,gastroenteritis infecciosa, otitis media supurada crónica y foliculitis severa).A la edad de 4 años 7 meses el paciente recibió –trece meses después de su ingreso– el trasplante de médula ósea, para lo cual fue preparado con busulfán y ciclosfosfamida. El cordón fue compatible con el paciente en 5/6 antígenos, la transfusión ocurrió sin incidentes y la nutrición se inició en forma parenteral. Hubo respuesta inflamatoria sistémica a los cuatro días del trasplante y se realizó en el catéter central un cultivo, el cual fue positivo para bacterias grampositivas, por lo que el paciente fue tratado con clindamicina, meropenem y vancomicina. Posteriormente, el paciente tuvo dificultad respiratoria secundaria a neumonía nosocomial por Staphylococcus aureus, por lo que ameritó intubación endotraqueal. Luego ingresó a terapia intensiva, donde 26 días después del trasplante falleció por choque séptico.
- El síndrome de Wiskott-Aldrich es causado por una mutación en el gen WASP, que codifica para la proteína del síndrome de Wiskott-Aldrich (WASp), presente sólo en las células hematopoyéticas. La proteína WASp es un regulador clave del citoesqueleto y de la señalización de múltiples funciones celulares, especialmente de la motilidad celular. El citoesqueleto, un conjunto de proteínas responsables de mantener la configuración de la membrana plasmática y la movilización y migración celular, está formado por filamentos de actina y miosina. La proteína WASp participa en la polimerización de la actina; cuando ésta resulta afectada, se impide la movilización celular a través de los filopodios y se produce ausencia de microfilamentos en las plaquetas, de ahí que éstas sean rápidamente destruidas en el bazo; también resulta afectada la fagocitosis
